La OMS define la esterilización como "la técnica de saneamiento cuya finalidad es la destrucción de toda forma de vida, aniquilando todos los microorganismos, tanto patógenos como no patógenos, incluidas sus formas esporuladas, altamente resistentes".
La esterilización supone el nivel más alto de seguridad o eficacia biocida en la destrucción de microorganismos o de sus formas de resistencia.
En contraposición, con la desinfección se eliminan los agentes patógenos reconocidos pero no todas las formas de vida microbianas y, con la limpieza, eliminamos la materia orgánica y contaminación de los objetos que es visible.
La higiene hospitalaria reúne el conjunto de técnicas y normas sanitarias destinadas a disminuir el riesgo de transmisión de enfermedades dentro del Hospital.
La asepsia es la ausencia de gérmenes que puedan provocar una infección o el procedimiento dirigido a impedir la llegada de microorganismos patógenos a un medio aséptico, previniendo la contaminación.
La antisepsia es el conjunto de actuaciones destinadas a eliminar los microorganismos patógenos presentes en un medio.
Por lo tanto, la asepsia previene la contaminación y la antisepsia la elimina una vez producida.
Los métodos de desinfección pueden dividirse de la siguiente forma:
- Métodos físicos:
- Ebullición: consiste en emplear el calor, dejando actuar sobre el material agua hirviendo a 100 ºC.
- Radiaciones ultravioletas: Oscilan entre los 2.000 y 3.000 Armstrong, se exponen directamente sobre la superficie.
- Pasteurización: se utiliza con líquidos para reducir la presencia en ellos de agentes patógenos. Fue utilizada por primera vez el 20 de abril de 1864 por Luis Pasteur (su creador) y Claude Bernard.
- Métodos químicos: Utilizan sustancias químicas para eliminar los gérmenes.
- Inmersión: Introducir los objetos en soluciones durante un determinado tiempo.
- Pulverización: Aplicación de la solución mediante pulverizadores sobre la superficie u objeto a desinfectar.
- Loción: Aplicación de la solución empapando mediante bayetas u esponjas, se utiliza para paredes, suelos, objetos o superficies.
- Fumigación: Aplicación de desinfectantes en forma de gas, humo o vapor.
- Aerosoles y brumas: Proyección de partículas pequeñas mediante aparatos, se utilizan en salas y locales.
Existen distintos tipos de desinfección, en función de los productos utilizados y su concentración:
- Desinfección de alto nivel: Se destruyen todos los microorganismos a excepción de algunas esporas bacterianas.
- Desinfección de nivel intermedio: Desactiva las bacterias vegetativas (incluido Mycobacterium Tuberculosis), la mayoría de virus y hongos, pero no destruye las esporas bacterianas.
- Desinfección de bajo nivel: Destruye la mayoría de bacterias vegetativas, algunos virus y hongos, pero no el Mycobacterium Tuberculosis ni las esporas bacterianas.
En función del uso que se le dé al instrumental podemos distinguir entre:
- Instrumental crítico: todo el que penetra en tejido estéril o sistema vascular del paciente. Requiere esterilización.
- Instrumental semi-crítico: todo aquel que, aunque no entra en contacto con tejido estéril ni sistema vascular, sí lo hace con mucosa o piel no intacta. Requieren desinfección de alto nivel.
- Instrumental y objetos no críticos: todos aquellos que entran en contacto con piel intacta. Requieren desinfección intermedia o de bajo nivel.
Como hemos comentado, la esterilización es la técnica de saneamiento cuya finalidad es la destrucción de toda forma de vida, aniquilando todos los microorganismos, tanto patógenos como no patógenos, incluidas sus formas esporuladas, altamente resistentes.
La esterilización puede llevarse a cabo a través de distintos agentes:
- Agentes físicos:
- Calor húmedo: a través del aparato llamado autoclave.
- Calor seco: utilizando métodos de incineración, flameado, estufa de Pasteur u horno de Poupinel.
- Radiaciones: utilizando rayos gamma, UV o infrarrojos.
- Agentes químicos:
- Gases: utilizando óxido de etileno o formaldehído.
- Líquidos: utilizando el glutaraldehído.
- Agentes mecánicos: utilizando ondas sónicas o ultrasónicas.
Esterilización por calor húmedo-vapor de agua: este método de esterilización utiliza el vapor de agua a presión para provocar la desnaturalización de los microorganismos por coagulación de sus proteínas.
Esterilización con gas óxido de etileno (OE): el OE es un agente microbiano de amplio espectro que destruye bacterias, esporas y virus. Se administra por gas, y actúa por alquilación, modificando la estructura molecular de las proteínas de los citados microorganismos.
Para el estudio del autoclave, reproducimos el contenido de la Guía para el Manejo del Autoclave del Grupo Español de Estudio sobre Esterilización, del Instituto Nacional de Gestión Sanitaria (ver documento original).
Un autoclave es un "recipiente metálico de paredes gruesas con cierre hermético que permite trabajar con vapor de agua a alta presión y alta temperatura que sirve para esterilizar material médico o de laboratorio".
El autoclave inactiva todos los virus y bacterias, aunque se ha llegado a saber que algunos microorganismos, así como los priones, pueden soportar las temperaturas del autoclave.
La olla de presión tiene el perfecto principio del autoclave.
La esterilización con vapor es el método más efectivo, actúa coagulando las proteínas de los microorganismos llevando así a su destrucción.
Existen unos controles de calidad de la esterilización:
- Control físico: Papel registrador, manómetros.
- Control químico: Cinta indicadora (indica solo si ha pasado por un proceso de esterilización). Tira de control interno o baliza se colocan en el interior y exterior de las cajas.
- Control biológico: Es el método de prueba más aceptado actualmente. Se realiza con esporas del Geobacilo Stearothermophilus, que es el microorganismo más resistente al calor.
La eficiencia de la esterilización con vapor está relacionada con la rapidez y la eficacia con que se remueve el aire de la cámara. Con el fin de detectar fallos en la remoción del aire dentro de la cámara apareció el test de Bowie-Dick. El aire atrapado dentro de la cámara del esterilizador es uno de los problemas más serios en el proceso de esterilización. Las fluctuaciones de la temperatura dentro de la cámara son frecuentemente signos de que el aire ha sido removido en forma incompleta.
Es muy importante para la esterilización que el vapor sea:
- Limpio: Es decir un vapor formado a partir de agua limpia, es decir, agua filtrada y libre de sustancias contaminantes como el cadmio, magnesio, plomo o cloro entre otras (agua osmotizada).
- Puro: Esto quiere decir que la presencia de agua en forma líquida sea muy baja, esto se considera cuando es menor al 3%.
Para que sea efectiva la esterilización:
- El vapor tiene que estar en contacto directo con el material a esterilizar (por lo que la carga de los elementos es muy importante).
- Debe crearse el vacío efectivo con el fin de desplazar todo el aire presente inicialmente en el autoclave y su sustitución por vapor.
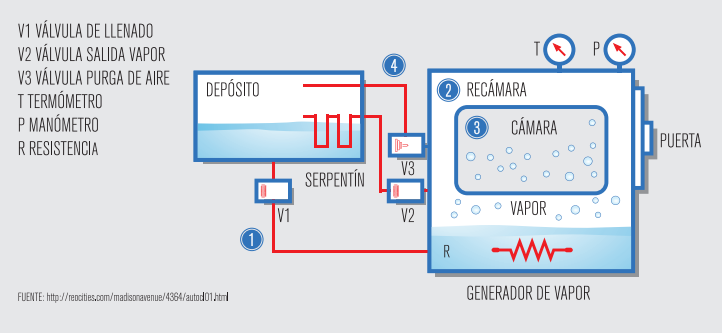
Para entender el funcionamiento de un autoclave, podemos atender a la siguiente imagen:
Las partes que componen un autoclave son las siguientes:
- Piloto indicador de falta de agua.
- Piloto línea.
- Apagador.
- Piloto termostato.
- Manómetro lector de presión en cámara.
- Manómetro lector de presión en camisa.
- Control central de operaciones.
- Puerta.
- Sistema de cerrado.
- Volante giratorio para abrir y cerrar la puerta.
- Termómetro lector de temperatura en cámara.
- Nivel de agua.
- Entrada de agua.
- Drenaje.
Durante un ciclo de esterilización, lo que sucede dentro del autoclave es lo siguiente:
- Paso del agua osmotizada desde el depósito hacia el generador de vapor: El agua osmotizada entra en el generador de vapor y una resistencia calentará ese agua y se generará el vapor libre de impurezas que se usará en la esterilización.
- Paso del vapor desde el generador hacia la recámara: Ese vapor pasa desde el generador de vapor a la recámara (habitáculo que rodea a la cámara, y la mantiene caliente), se trata de un mecanismo neumático, quiere decir, que necesita aire comprimido para la apertura de la llave de paso.
- Paso de la recámara a la cámara: Es el sistema que permite el paso de vapor desde la recámara hacia la cámara en función de las necesidades. Se trata de un mecanismo neumático que necesita aire comprimido para su funcionamiento. La cámara: habitáculo donde se dará el proceso de esterilización.
- Purga de aire (Sistema de vacío): Es el sistema que se encarga de realizar el vacío en la cámara para poder de esta forma eliminar el aire contenido en la cámara inicialmente.
Las etapas del ciclo de esterilización, donde se esteriliza con vapor de agua saturado exeno de aire, son las siguientes:
- Marcha: Se cierran las puertas herméticamente para que la cámara quede estanca.
- Purga de aire: En esta fase se eliminara el aire contenido en la cámara y se favorecerá a la eliminación posterior del aire dentro de los paquetes y de los contenedores. Para ello se inyecta vapor en la cámara y se activa el sistema de vacío.
- Preparación: Para la extracción del aire de los productos y de la cámara, se realiza una serie de fases (hasta cuatro) de inyección de vapor (de recámara a cámara) seguidas de fases de vacío (prevacío), mediante el sistema de vacío, para eliminar completamente el aire restante.
- Calentamiento: Se introduce vapor en la cámara y en el interior de los contenedores, hasta alcanzar la temperatura y presión de esterilización.
- Esterilización: Se mantiene constante la temperatura y presión en la cámara durante el correspondiente tiempo de esterilización.
- Desvaporización: El vapor de la cámara es eliminado por el sistema de vacío y se produce un descenso de la presión.
- Secado: Se inicia un vacío final, profundo y duradero. Se mantiene el vapor en la recámara, para mantener caliente la cámara y ayudar a secar el producto a fin de evitar todo tipo de recontaminación bacteriana durante el transporte y el almacenamiento.
- Igualación: Entrada de aire atmosférico a la cámara, a través de un filtro de aire estéril, para compensar la presión de la cámara (que estaba en depresión) con la atmosférica. El vapor utilizado se condensa y se convierte en agua transportándose a un depósito.
- Finalización del proceso: Se liberan las puertas para que puedan ser abiertas.
Los materiales que se esterilizan a través de este método son:
- Textiles (batas, paños, gasas...)
- Elementos duros: envases o recipientes.
- Material de vidrio o cristal.
- Líquidos hidrosolubles no alterables por el calor.
- Elementos de metal no alterables por el calor.
- Elementos de goma o silicona.
La esterilización por calor seco es menos eficaz que la realizaba en el autoclave y se utiliza principalmente para la esterilización de vidrio y material de laboratorio, polvos y sustancias oleosas.
Existen tres métodos de esterilización por calor seco:
- Flameado: en el que se aplica una llama al objeto a desinfectar. Se utiliza para esterilizar objetos pequeños, pero no puede utilizarse en tijeras, bisturís, pinzas o agujas, porque se destemplarían y perderían su filo.
- Incineración: en el que se eliminan al completo los objetos, a través de su combustión directa o de un horno crematorio. Se utiliza para objetos de un solo uso que deben destruirse al completo, como contenedores con material biológico contaminado, vendas, lencería o restos orgánicos.
- Horno de calor seco Pasteur o Estufa Poupinel: en el que se eliminan las bacterias a través de la oxidación física o coagulación de las proteinas bacterianas al aplicarles calor. Para conseguir que se eliminen se debe exponer el material a esterilizar a la acción del calor durante largos periodos de tiempo. La relación de temperatura / tiempo que debe utilizarse es la siguiente:
- 180° C / 30 minutos.
- 170º C / 70 minutos.
- 160º C / 120 minutos.
- 150º C / 150 minutos.
- 140° C /180 minutos.
El ácido peracético es un agente oxidante resultante de la mezcla de ácido acético y peróxido de hidrógeno en solución acuosa.
La esterilización por ácido peracético se hace introduciendo los materiales a esterilizar en bandejas dentro de STERIS (una máquina de esterilización), que utiliza el ácido peracético envasado combinado con bajas temperaturas para eliminar y destruir los microoganismos.
Normalmente, se utiliza un 2% de ácido peracético, dejándolo actuar a 35ºC durante 18 minutos.
La esterilización por vapor a baja temperatura con formaldehído al 2% es un nuevo método de esterilización que se utiliza para material termosensible (sensible y vulnerable por la temperatura).
Se utiliza, por lo tanto, para material de plástico, catéteres y sondas reutilizables, endoscopios, sistemas ópticos, cables de luz endoscópicos, etc; aunque no se recomienda su uso para los materiales de látex porque absorben el formaldehído en exceso. Tampoco pueden utilizarse en materiales que no aguantan una humedad relativa media del 90%.
Este método presenta algunas ventajas, entre las que destacamos su facilidad de uso, que no generan residuos tóxicos y que tienen un clico más rápido de esterilización.
Este método de esterilización se lleva a cabo envolviendo y precintando los materiales y puede desarrollarse:
- A una temperatura de 50ºC durante 5 horas.
- A una temperatura de 60ºC durante 3 horas.
La esterilización con óxido de etileno (OE) se utiliza para la esterilización del material médico y quirúrgico que es sensible al calor y que no resistiría otros procesos de esterilización por sus altas temperaturas.
El óxido de etileno tiene una gran capacidad germinicida y de difusión, que le permite alcanzar las zonas más estrechas de los materiales.
Debe tenerse cautela en su utilización, ya que puede provocar efectos sobre la salud de las personas, como irritación cutánea y de las mucosas. Si la exposición es prolongada puede llegar a provocar irritación en los ojos, nariz y garganta, sequedad de la boca, náuseas o vómitos y neuralgias o y cefaleas.
Para el estudio de la esterilización con óxido de etileno (OE), reproducimos en los siguientes apartados el contenido de la NTP 470: Óxido de etileno: prevención de la exposición en hospitales del Ministerio de Trabajo y Asuntos Sociales (actual Ministerio de Trabajo, Migraciones y Seguridad Social). Ver documento original.
Solo se utiliza el óxido de etileno para esterilizar materiales que no sean capaces de resistir más de 115 ºC, temperatura mínima a la cual se efectúa la esterilización por el autoclave de vapor.
Los materiales que nunca deben esterilizarse con óxido de etileno son los siguientes:
- Líquidos, gases, o productos sólidos que puedan cambiar su composición química por acción del OE.
- Materiales plásticos impregnados con agua, lubricantes u otras sustancias químicas.
- Materiales muy absorbentes (textiles, celulosas).
- Materiales envueltos con gasas u otros textiles.
- Materiales que estén fabricados con Mg, Zn o Sn ya que se deterioran con el OE.
- Nylon y papel de aluminio (que tampoco deben utilizarse para envolver o empaquetar otros materiales).
- El metacrilato y caucho porque retienen altas cantidades de óxido de etileno.
- De manera general, se recomienda no reesterilizar con OE materiales de PVC previamente esterilizados con rayos gamma, por existir riesgo de formación de clorhidrina.
Acciones previas al proceso
El material debe someterse a una limpieza minuciosa para eliminar todos los restos de materia orgánica y enjuagar abundantemente los materiales una vez limpios. El material debe estar totalmente seco ya que el óxido de etileno en presencia de agua se hidroliza rápidamente formando etilenglicol.
Una vez los materiales están limpios y secos deben ser embolsados en papel mixto (plástico y papel) o en con tenedores metálicos, nunca en textil, debido a su capacidad absorbente. Las bolsas serán colocadas verticalmente en cestas de alambre de manera holgada, de modo que siempre esté en contacto papel plástico, con el fin de favorecer la difusión del gas hasta los materiales que se van a esterilizar.
Acciones durante el proceso
Durante el proceso de esterilización se llevan a cabo una serie de controles que permiten comprobar el correcto funcionamiento del autoclave y del proceso de esterilización:
- Control físico del autoclave a través de los gráficos y manómetros del autoclave.
- Control químico del proceso de esterilización a través de tiras colorimétricas de las que se coloca una en cada paquete.
- Control biológico de la eficacia de esterilización. Se realiza a través de esporas inoculadas.
Acciones posteriores al proceso
Una vez finalizado el ciclo, todos los materiales deben ser aireados durante 12 horas como mínimo, a la misma temperatura que se ha realizado el ciclo. Este proceso de aireación puede tener lugar en el propio autoclave una vez terminado el ciclo de esterilización o en las cabinas de aireación diseñadas específicamente para este fin.
En este caso el paso del material del autoclave a la cabina de aireación, se hará de manera inmediata y sin etapas intermedias y se utilizará siempre: mascarilla específica, gorro, guantes y gafas. Los equipos de protección individual deben llevar la etiqueta CE y el folleto del fabricante debe especificar su adecuación para la protección frente al OE.
Transcurrido el período de aireación, se coloca el material en la zona estéril listo para poder ser utilizado.
Antes de su entrega se comprobará que los controles químicos y biológicos hayan proporcionado un resultado correcto.
La exposición de los trabajadores a óxido de etileno puede tener lugar principalmente durante las siguientes operaciones o situaciones:
- Al sacar la carga una vez finalizado el ciclo, especial mente si ésta no ha sido previamente aireada.
- En la zona del almacenamiento del material esterilizado por la desorción de óxido de etileno residual del material esterilizado.
- En la conexión, abertura y manipulación de las botellas de gas.
- Posibles situaciones de emergencia o accidente que pueda ocurrir.
Como hemos comentado anteriormente, el óxido de etileno es un gas extremadamente inflamable y tóxico; en consecuencia, habrá que tomar todas las precauciones necesarias, tanto durante su almacenamiento como su uso, así como tener el procedimiento de actuación para casos de emergencia.
Las acciones preventivas para reducir al máximo la exposición a óxido de etileno se pueden resumir en las siguientes:
- Prohibición de comer, beber y fumar en toda el área de trabajo.
- Sólo se esterilizarán con óxido de etileno aquellos materiales que no se puedan esterilizar con el autoclave de vapor.
- La unidad de esterilización será una zona de paso restringido y solamente estará permitida la entrada al personal del servicio. Deberá, por tanto, estar convenientemente señalizada.
- La puerta de la zona donde está ubicado el óxido de etileno debe permanecer cerrada.
- Las intervenciones del personal de mantenimiento y limpieza se deberán hacer en condiciones de mínimo riesgo (máquinas paradas, días libres) y siempre después de haberles informado y dándoles los equipos de protección personal adecuados. De manera general, es recomendable que se consideren trabajos con autorización.
- El sistema de ventilación debe funcionar correctamente, por lo que deben realizarse los controles adecuados.
- Para asegurarse de que el autoclave funciona y la esterilización es correcta se debe:
- Controlar los parámetros físicos del sistema automático.
- Colocar en cada bolsa un control químico.
- Realizar en cada ciclo un control biológico.
- El autoclave se utilizará siempre siguiendo las instrucciones del fabricante.
- Tanto las máquinas como las instalaciones deberán tener un protocolo de mantenimiento.
- El material dentro de las cestas se colocará vertical mente y siempre de modo que coincida papel con plástico.
- Se procurará que las cestas no estén completamente llenas, quedando holgadas.
- Se respetará el período de aireación del material, que será como mínimo de 12 horas.
- Para entrar en la zona del OE se utilizarán batas de protección de uso exclusivo para esta zona.
- Para abrir el autoclave el personal se colocará: guantes, mascarilla, gorro y gafas.
- Una vez terminado el proceso de esterilización y de aireación se procederá al almacenamiento del mate rial a las condiciones adecuadas.
- Los cartuchos vacíos se introducirán en el aireador o se les añadirá agua para eliminar el óxido de etileno residual que pueda quedar. Una vez tratado, el cartucho se eliminará como residuo urbano.
- No se almacenarán más de seis cartuchos, ya que es un gas muy inflamable, sin tomar las debidas precauciones. Es recomendable ubicarlos en un lugar seguro, alejados de focos de ignición y de calor y, preferiblemente, en un armario para inflamables.
- Siempre que se sospeche un funcionamiento incorrecto del proceso de esterilización debido al cartucho, por ejemplo, y tenga que manipularse el mismo una vez esté conectado, se emplearán los equipos de protección individual correspondientes, básica mente guantes y mascarillas
- Si se observa algún cartucho defectuoso se devolverá al suministrador.
- Hay que disponer de instrucciones detalladas de los pasos a seguir en caso de emergencia (fuga, incendio, etc.).
- Se recomiendan controles ambientales y persona les periódicos con el fin de conocer los niveles residuales de óxido de etileno. Se efectuará una evaluación ambiental cuando se sospeche que hay una fuga.
- Es indicado disponer de una alarma sonora y visual que se active en caso de fuga o nivel de contaminación elevado.
Existen numerosos procedimientos para realizar la esterilización por óxido de etileno (OE), la mayoría de ellos incluyen tres fases o etapas diferenciadas:
- Fase de acondicionamiento previo: destinada a que la cantidad de microorganismos que se encuentran en los materiales crezca, realizando una carga por lotes en un entorno con temperatura y humedad controlados.
- Fase de esterilización: es la fase donde se produce la esterilización. Durante esta, debemos prestar atención a la precisión del control término. Su duración es de 60 horas aproximadamente. También es imprescindible controlar, en todo momento, el vacío y la presión.Durante esta fase se genera un informe, controlando la tolerancia de los microorganismos, los cambios de fase y las alarmas o valores críticos que suceden durante el proceso. Este informe se imprime y almacena electrónicamente para su futura consulta o referencia. Se podrán realizar búsquedas en base a:
- ID del lote.
- Nombre del cliente/servicio.
- Receta.
- Tipo de producto.
- Hora de inicio y finalización.
- Fase de desgasificación: es la fase en la que se eliminan los restos de óxido de etileno de los materiales esterilizados.
El glutaraldehídico se utiliza como desinfectante frío y esterilizador en materiales sensibles al calor como instrumentos de diálisis y cirugía, frascos de succión, endoscopias o instrumental para el oído, nariz y garganta.
Normalmente se utiliza diluido en agua, con una concentración de entre el 1% y el 50%.
Para el estudio de la esterilización con glutaraldehídico, reproducimos en los siguientes apartados el contenido de la NTP 506: Prevención de la exposición a glutaraldehídico en hospitales del Ministerio de Trabajo y Asuntos Sociales (actual Ministerio de Trabajo, Migraciones y Seguridad Social). Ver documento original.
El personal de los hospitales expuesto a esta sustancia es el que trabaja en las áreas donde se utiliza para la limpieza y desinfección, en concreto:
- Quirófanos, diálisis, unidades de endoscopia y UCIS.
- Servicio central (suministros).
- Técnicos de investigación, investigadores y personal de farmacia.
- Técnicos de laboratorio.
- Trabajadores que revelan rayos X.
En los quirófanos se realizan dos niveles de limpieza, una entre intervención e intervención y otra más a fondo, que se suele llamar limpieza terminal, al final de la jornada laboral, consistente en las siguientes acciones:
- Vaciado de los contenedores de residuos en las bolsas de plástico utilizadas. Estas bolsas se cierran con doble nudo y se evacuan para su eliminación según el plan de gestión de residuos sanitarios del centro.
- Cierre del quirófano durante un tiempo para que el aire quede en reposo con el fin de que puedan sedimentar las partículas en suspensión.
- Si en el suelo del quirófano hay manchas de sangre, pus u otros líquidos orgánicos, se hace una primera limpieza con agua, detergente y lejía (100 ml de lejía en 10 l de agua). Una vez eliminadas estas manchas se tira el agua y se aclara el cubo con agua limpia.
- Limpieza del mobiliario con la solución de aldehídos a la concentración que se indique el protocolo específico (normalmente suele ser del 1%). A continuación sigue la de las superficies horizontales (mesa de operaciones, mesas auxiliares e instrumental), la de las verticales del mobiliario y, finalmente, las paredes, siempre de arriba abajo.
- Una vez concluida la limpieza de mobiliario y paredes se inicia el fregado y desinfección de suelos. 6. Al finalizar la limpieza se tira el agua del aclarado de la gamuza y la solución utilizada para la limpieza, de tal manera que al iniciar una nueva limpieza se utilice siempre agua y solución totalmente limpias.
Al glutaraldehído se le considera un producto irritante y también sensibilizante. En exposiciones de corta duración y aun a bajas concentraciones, produce irritación de las mucosas y especialmente del tracto respiratorio superior, aunque a este respecto debe tenerse en cuenta su baja presión de vapor (recuérdese que su punto de ebullición es cercano a 200ºC).
Por lo que se refiere al contacto dérmico con soluciones conteniendo glutaraldehído, no se han descrito efectos irritantes a concentraciones inferiores al 0,5% ni tampoco sensibilización a concentraciones inferiores a 0,1%.
El contacto prolongado o repetido con la piel a concentraciones más elevadas puede producir dermatitis y sensibilización.
El proceso de esterelización debe someterse a controles periódicos de calidad, que pueden ser:
- Controles físicos: a través de elementos de medida incorporados a la autoclave: termómetro, manómetro, válvulas, etc que permiten visualizar si se alcanzan los parámetros necesarios para llevar a cabo la esterilización.
- Controles químicos: a través de tiras y cintas adhesivas impregnadas con sustancias químicas no tóxicas que reaccionan mostrando un color de blanco a negro al entrar en contacto con el agente esterilizarte. Estos nos indican si el objeto ha sido esterilizado, distinguiendo entre procesados (esterilizados) y no procesados (no esterilizados).
- Controles químicos procesados: a través de bandas en las bolsas de los objetos que deben esterilizarse, que cambian de color cuando se procesan en la autoclave.
- Controles biológicos: a través de viales con carga suficiente de esporas de alta resistencia a la esterilización (Geobacillus Stearothermophilus) que demuestran que la esterilización se ha llevado a cabo de forma satisfactoria cuando se destruyen por completo.
Al sacar el objeto de la incubadora, el resultado tiene que ser siempre negativo, si apareciese un resultado positivo, querría decir que el proceso de esterilización no se ha completado con éxito y que la espora ha crecido, en lugar de eliminarse por completo. Los resultados se pueden leer pasadas:
- 24 horas, si nos basamos en el cambio de color del medio de cultivo.
- 3 horas, si se trata de incubadoras de lectura rápida.
Prueba de Bowie-Dick
Se realiza diariamente en los esterilizadores pre-vacío y sirve para valorar su capacidad de:
- Extracción de aire de la cámara.
- Penetración del vapor de agua.
- Vapor súper calentado.
- Presencia de gases no condensables.
Esta prueba debe realizarse, además, de forma previa al primer ciclo operativo del día, con la cámara vacía y tras un ciclo previo de calentamiento. Si se tratase de autoclaves utilizadas durante las 24 horas, esta prueba puede hacerse en cualquier momento del día, pero todos los días a la misma hora.
Este test nos puede alojar dos resultados:
- Si el test es correcto: la hoja cambia de color de forma uniforme, totalmente, de amarillo a negro. Esto nos indicaría que tiene suficiente temperatura, tiempo y penetración de vapor.
- Si el test es incorrecto: el cambio de color de la hoja no es uniforme. Debemos repetir la prueba una vez y, si vuelve a salir como no correcta, deberemos dejar la autoclave fuera de servicio y avisar al equipo técnico. Esto nos indicaría que no tiene suficiente extracción de aire y penetración de vapor y que la temperatura no es correcta.
Es importante que, a la hora de elegir el agente esterilizante que vamos a utilizar, primemos algunas características básicas:
- Alta eficacia.
- Rápida efectividad en el menor tiempo posible.
- Penetrabilidad.
- Compatibilidad.
- Ecoseguridad (respeto al medio ambiente).
- Adaptabilidad.
- Monitorización.
- Eficacia y costes.
Además, en todo momento, debemos tratar de reducir los riesgos de exposición, tanto respecto a instrumental y materiales delicados como a las propias personas.
Con respecto a la unidad de esterilización, corresponden al celador las siguientes funciones:
- Reponer los sobres que falten en las estanterías.
- Recoger el material procedente de los distintos servicios, por ventanilla, plantas y consultas, y por los elevadores procedentes del quirófano.
- Revisar los elevadores de la zona «de sucio» de acuerdo con el horario establecido y siempre que se reciba aviso de envío de material.
- Descargar las autoclaves cuando terminen los ciclos.
- Colocar en los contenedores de instrumental, las etiquetas con la fecha de esterilización y el número de autoclave en el que han sido esterilizados.
- Llamar a los quirófanos para que retiren el material de los elevadores.
- Descargar los carros procedentes de lencería.
- Colocación del material fungible procedente de los almacenes.
- Descargar los elevadores de “ sucio” para esterilizar.
- Transportar el material esterilizado de los diferentes pabellones a la central y viceversa.
- Llevar las esporas (flora bacteriana) a bacteriología, para su análisis (tiras de papel inoculado con bacilos resistentes a cada tipo de esterilización).
- Llevar los pedidos de ropa, sobres y rollos de cinta de precintar que soliciten los quirófanos.
- Mantener la limpieza y el orden en el lugar de trabajo.
- No entregar absolutamente nada sin vale o autorización de la supervisora.
La "Guía de recomendaciones para el control de la infección nosocomial" prevé una seria de condiciones generales para la correcta aplicación de los métodos de esterilización, los cuales, hemos englobado en el siguiente cuadro de referencia:
| Condiciones generales para la correcta aplicación de los métodos de esterilización | |
|---|---|
| Limpieza | El material a esterilizar debe estar
|
| Empaquetado | El material a esterilizar por vapor u óxido de etileno (O.E.) debe estar empaquetado
|
| Compatibilidad con los materiales a esterilizar | La morfología de éstos debe permitir el acceso del agente esterilizante a todas las partes y superficies a esterilizar, no debiendo deteriorarse el material en cuanto a su
Antes de adquirir cualquier material, instrumental, etc., debería exigirse al fabricante cual es el método de elección para su esterilización, prefiriéndose siempre aquellos que permitan la esterilización por vapor de agua |
Transporte | En bolsa de plástico transparente y en carro cerrado |
Almacenamiento | El material estéril debe almacenarse en zona limpia y no mezclarse con otros materiales |
| Caducidad | El material almacenado en estantes al aire o en armario cerrado tendrá una caducidad distinta según el tipo de envoltorio externo y selladura:
Se considerará caducado cualquier paquete que haya perdido su integridad física |
| Etiquetado | El material debe etiquetarse haciendo constar
El etiquetado debe ser doble para que figure en el parte quirúrgico (trazabilidad) |
| Controles de calidad | Las condiciones físicas (temperatura, humedad, presión ...) de los métodos de esterilización deben poder registrarse en cada ciclo, así como el tiempo de esterilizado. Todos los paquetes y cajas esterilizados deben disponer de controles químicos que permitan comprobar que han sufrido un ciclo de esterilización. Deben realizarse controles biológicos con una frecuencia que dependerá del método utilizado. Se llevará un libro de registro de controles e incidencias, así como de las revisiones periódicas |
| Organización | Es aconsejable centralizar los procesos de esterilización en unidades específicas |
| Prevención de riesgos | Según el método utilizado se deberán establecer medidas de control para prevenir los posibles riesgos de toxicidad para trabajadores y pacientes |
En cuanto a los métodos de esterilización, la "Guía de recomendaciones para el control de la infección nosocomial" , indica que sólo se consideran recomendables aquellos métodos en los que las condiciones de aplicación son validables, y además pueden realizarse controles de calidad del proceso.
Entre los principales métodos de esterilización podemos observar los siguientes que agrupamos en el siguiente cuadro explicativo:
| Métodos de esterilización | |
|---|---|
Calor húmedo (autoclave vapor) Calor seco, (Poupinel) Óxido de etileno Gas plasma de peróxido de hidrógeno Vapor a baja temperatura y Formaldehído Ácido peracético (Steris System1) | |
Limpieza y esterilización del material utilizado en pacientes con enfermedad (o sospecha clínica) de Creutzfeldt-Jakob u otras encefalopatías espongiformes |
Calor húmedo (autoclave vapor)
- Para material termorresistente como textil, instrumental, cauchos, guantes y plásticos, además es le método más barato, rápido y seguro.
- En el empaquetado y carga se debe vigilar la penetrabilidad del vapor de agua, y los paquetes mojados deben desecharse.
- Además del registro de las condiciones físicas (temperatura y presión) y del tiempo de cada ciclo, se realizará, al inicio de cada jornada y después de cada avería, una prueba que verifique el buen estado del autoclave.
- Los controles biológicos serán, preferiblemente diarios y como mínimo, semanales.
- Existen dos ciclos estándar
- Para material de caucho a 121º C, 1 atmósfera de presión y duración de 15 - 20 minutos
- Para textil e instrumental a 135ºC, 2 atmósferas y una duración de 5 a 10 minutos
- El programa flash se utiliza en miniclaves de vapor en el quirófano, el cual, se deberá usar exclusivamente para emergencias con instrumental necesario en un momento puntual del acto quirúrgico. Se efectuará siempre con este instrumento envuelto en paño verde.
- El miniclave se someterá a controles y validación del ciclo periódicamente.
- Las autoclaves deben ser revisadas técnicamente al menos una vez al año y siempre que se detecten alteraciones en los ciclos, registrándose la temperatura interior y comprobándose la calidad del vapor y validándose el ciclo. Dichas revisiones se harán constar en el libro de registro.
- Es un método eficaz frente a priones.
Calor seco, (Poupinel)
Es un sistema que elimina microorganismos por coagulación de las proteínas.
- Está recomendado de manera exclusiva para ciertos materiales de farmacia y laboratorio, además requieren mayor tiempo de esterilización que el calor húmedo y temperaturas más altas.
- No es un método eficaz frente a priones.
Óxido de etileno
El óxido de etileno (ETO, en inglés) a temperatura ambiente es un gas incoloro, inflamable y de olor dulce, que está clasificado por el Reglamento (CE) nº 1272/2008 como un posible mutágeno, posible carcinógeno y posible tóxico para la reproducción, pudiendo tener estos potenciales efectos en el organismo.
- Es el método más utilizado para el material termosensible, señalando que el óxido de etileno puro sigue siendo un método altamente eficaz.
- La temperatura del ciclo (35ºc- 55ºc), características de tiempo y humedad dependen de la mezcla de óxido de etileno.
- De acuerdo con lo establecido en la Directiva del Consejo Europeo 90/394/CEE, los aparatos se han adaptado a las nuevas mezclas denominadas OXYFUME 2000 (8,6% OE y 91,4 HCFC-124) y OXYFUME 2002 (10% OE, 63% HCFC-124 y HCFC-22), cuya producción está asegurada hasta el año 2015.
- El óxido de etileno es un gas tóxico que obliga a eliminar sus restos del material esterilizado, esto se consigue mediante la aireación forzada y a 60º C durante 8 horas, como mínimo.
- Para el empaquetado no debe utilizarse tela.
- Para controlar el proceso de esterilización, además de los indicadores químicos en cada paquete o caja, se harán controles físicos y biológicos en cada programa.
- Las cámaras deberán recibir una revisión técnica, al menos anualmente, y siempre que se detecten alteraciones en los ciclos, tras ella se validará el ciclo y se hará constar en el libro de registro.
- Por la toxicidad del Óxido de etileno, las instalaciones deben estar acondicionadas para evitar la exposición de los trabajadores, estableciéndose los controles necesarios.
- Indicar que no es un método eficaz frente a priones.
Gas plasma de peróxido de hidrógeno
El plasma de peróxido de hidrógeno es un modo de esterilización de tipo químico, que convierte el peróxido de hidrógeno en el cuarto estado de la materia que es el plasma, mediante ionización.
- Es otro método para material termosensible.
- El gas plasma se considera el cuarto estado de la materia (además de sólido, líquido y gaseoso), consistente en una nube de iones, electrones y partículas atómicas neutras.
- El sistema Sterrad utiliza plasma a baja temperatura a partir de vapor de peróxido de hidrógeno. Tras el proceso de esterilización se produce oxígeno y agua, por lo que no requiere aireación posterior. La temperatura es de 45ºC y la humedad es mínima.
- Actualmente los ciclos son de 54 y 72 minutos. Dispone de controles físicos, químicos y biológicos especialmente diseñados. El proceso no sirve para:
- Materiales de celulosa o derivados
- Material de hilo
- Polvos o líquidos
- El material de empaquetado debe ser compatible con este sistema. Los artículos de cabo ciego (romos sin lumen) de tamaño superior a 30 cm presentan problemas de esterilización con este sistema. Para los utensilios huecos de pequeño calibre (<3mm) de más de 2 m si son flexibles y de más de 1 m si son rígidos, existen adaptadores que garantizan el proceso de esterilización. El material a esterilizar debe estar perfectamente limpio y seco para que no se aborten los ciclos.
- La caducidad de los paquetes de 1 a 5 años.
- No es eficaz frente a priones.
Como se ha establecido en el apartado anterior, la "Guía de recomendaciones para el control de la infección nosocomial" establece junto al calor húmedo, calor seco, el gas plasma de peróxido de hidrógeno y el óxido de etileno, lo siguientes métodos de esterilización:
Vapor a baja temperatura y Formaldehído
- Es otro método para material termosensible, que utiliza formaldehído al 2% con vapor de agua al 95% en vacío.
- Los ciclos pueden ser a 60ºC y 50ºC con una duración de 3 horas y 5 horas respectivamente. Los aparatos disponibles incluyen al finalizar el ciclo una fase de extracción de la mezcla vapor/formaldehído, de tal manera que no será necesario una aireación suplementaria.
- Dispone de controles físicos, químicos y biológicos. El material de empaquetado debe ser compatible con el sistema. El material a esterilizar debe estar perfectamente y limpio.
- El formaldehído es una sustancia tóxica, existiendo poca experiencia documentada sobre la exposición del personal.
- No es eficaz frente a priones.
Ácido peracético (Steris System1)
Es un compuesto orgánico con la fórmula CH3CO3H también conocido como ácido peroxiacético, es un producto de reacción de equilibrio que se produce por la reacción de ácido acético con peróxido de hidrógeno.
- Es un sistema húmedo, de esterilización químico por inmersión, a baja temperatura (50º-55ºC) en un espacio corto de tiempo, que emplea cartuchos precargados de ácido peracético al 35% junto con neutralizante (dilución final de uso 0,2%). El tiempo del proceso es de 25-30 minutos. El sistema es monitorizado con controles físicos, químicos, con registro impreso. Los ciclos pueden validarse con controles biológicos. Diseñado fundamentalmente para material endoscópico en punto de uso, es de gran utilidad cuando el material tiene un elevado índice de utilización.
- Debe tenerse en cuenta que el material a esterilizar debe estar absolutamente limpio.
- El material esterilizado no puede ser empaquetado ni se puede almacenar.
- No es un método eficaz frente a priones.
Limpieza y esterilización del material utilizado en pacientes con enfermedad (o sospecha clínica) de Creutzfeldt-Jakob u otras encefalopatías espongiformes
Para el material reutilizable, las pautas a seguir dependerán de si se ha utilizado en procedimientos de riesgo demostrado. Las indicaciones de las pautas a seguir según los procedimientos sean de riesgo demostrado o no, deben ser consultados con los servicios de Medicina Preventiva. El material utilizado debe desecharse en contenedores de residuos grupo IV.
- Limpieza:
Debe realizarse por personal formado y protegido con guantes, bata, mascarilla y gafas, durante toda la operación de limpieza, tanto si es manual como mecánica. El material debe mantenerse húmedo hasta su limpieza y descontaminación. Debe limpiarse lo antes posible después de utilizarlo, separado del resto de material clínico, no debiendo mezclar instrumentos usados en tejidos de infectividad no detectable, con aquellos utilizados sobre tejidos de alta o baja infectividad. Está formalmente contraindicado utilizar productos que contengan aldehídos (formol, glutaraldehído), ya que tienen una acción protectora de estos agentes frente a los procedimientos de inactivación empleados ulteriormente. Si se utilizan máquinas automáticas, el instrumental debe descontaminarse previamente con un método adecuado, realizando un ciclo vacío, antes de volver a utilizarse. En caso de utilización de una cubeta de ultrasonidos, habrá que verificar la compatibilidad del producto. La fase de limpieza es muy importante, ya que reduce notablemente la carga de infectividad y condiciona la eficacia de etapas ulteriores. Sin embargo, el material limpio puede estar todavía contaminado.
- Inactivación:
Los métodos de inactivación recomendados por la OMS en orden de más a menos severos son:
1. Incineración
Usar para todo instrumental y material desechables y otros residuos. Es el método de elección para todo instrumental expuesto a tejidos de alta infectividad.
Utilizar contenedores para residuos grupo IV.
2. Autoclave/métodos químicos para instrumental resistente al calor
- a) Inmersión en NaOH (1N) y calor en autoclave de desplazamiento por gravedad a 121ºC 30 min; limpiar; aclarar con agua y someter al procedimiento rutinario de esterilización.
- b) Inmersión en NaOH (1N) o Hipoclorito sódico (20.000 ppm) durante 1 hora; transferir el instrumental a agua; someter a 121ºC en autoclave de desplazamiento por gravedad durante 1 hora; limpiar y someter al procedimiento rutinario de esterilización.
- c) Inmersión en NaOH (1N) o Hipoclorito sódico (20.000 ppm) durante 1 hora; sacar y clorar con agua, entonces transferir a un contenedor abierto y someter a 121ºC en autoclave de desplazamiento por gravedad o a 134ºC en autoclave de carga porosa, durante 1 hora; limpiar y someter al procedimiento rutinario de esterilización.
- d) Inmersión en NaOH(1N) y ebullición durante 10 min a presión atmosférica; limpiar; aclarar con agua y someter al procedimiento rutinario de esterilización.
- e) Inmersión en Hipoclorito sódico (20.000 ppm) (preferible) o a NaOH (1N) (alternativa) a temperatura ambiente durante 1 hora; limpiar; aclarar con agua y someter al procedimiento rutinario de esterilización.
- f) Autoclave a 134ºC durante 18 minutos.
3. Métodos químicos para superficies e instrumentos sensibles al calor
- a) En suelos utilizar NaOH (2N) o hipoclorito sódico sin diluir; dejar por 1 hora; fregar y aclarar con agua.
- b) Para superficies que no toleran ni el NaOH ni el Hipoclorito sódico, la limpieza puede eliminar por dilución gran parte de la infectividad y puede utilizarse algún método parcialmente efectivo.


No hay comentarios:
Publicar un comentario